

Molte ricerche hanno scoperto che una mutazione al gene MTHFR (che colpisce il 10-15% dell’intera popolazione) può portare a tantissimi problemi.
Che magari rimangono misteriosi proprio perchè quasi nessuno prescrive il test per scoprirlo.
Come sapere se ne sei in possesso e cosa fare per limitarne/bloccare i possibili danni.
Scopri se hai questa mutazione con un semplice test salivare.
Claudio Tozzi
Il nome è improponibile da pronunciare e cioè “metilenetetraidrofolato reduttasi (o MTHFR)”, ma può dare veramente dei grossi problemi.
Si tratta di un enzima che scompone gli aminoacidi omocisteina e folati, una particolare forma di acido folico, una vitamina del gruppo B.
Infatti, se il gene MTHFR che codifica per questo enzima è mutato, può interferire con la capacità di quest’ ultimo di funzionare normalmente o inattivarlo completamente.
E queste mutazioni dei geni MTHFR si verificano in milioni di persone e cioè circa il 25% delle persone di origine ispanica e nel 10-15% delle persone di origine europea.
Quindi in Italia ci sono circa 6-9 milioni di persone che potenzialmente posso avere delle conseguenze più o meno gravi a causa di questa mutazione.
Forse anche tu.
Queste mutazioni portano spesso a livelli elevati di omocisteina nel sangue, che possono contribuire a numerose condizioni di salute, come:
- anomalie alla nascita
- malattie cardiovascolare
- glaucoma
- disturbi di salute mentale
- alcuni tipi di cancro
Le persone hanno due geni MTHFR, ereditando uno da ciascuno dei loro genitori.
Le mutazioni possono interessare uno (eterozigote) o entrambi (omozigoti) di questi geni.
Esistono due tipi comuni o varianti di mutazioni MTHFR: C677T e A1298C.
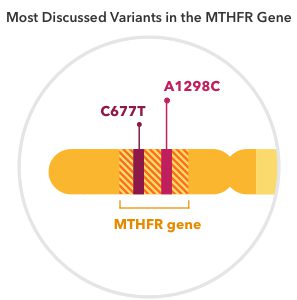
Le persone ereditano una copia del gene MTHFR da ciascuno dei loro genitori, il che significa che tutti hanno due geni MTHFR. Le mutazioni possono verificarsi in uno o entrambi i geni.
Avere un genitore o un parente stretto con una mutazione del gene MTHFR può aumentare il rischio di una persona di ereditare la stessa variante.
Le persone che hanno due genitori con mutazioni hanno un rischio maggiore di avere una mutazione MTHFR omozigote.
Per far comprendere meglio le problematiche che possono scaturire, esaminerò le mutazioni MTHFR in modo più dettagliato, comprese le relative condizioni di salute, come viene diagnosticata e opzioni di trattamento.
Le mutazioni MTHFR possono influenzare anche la gravidanza.
Condizioni legate alla mutazione MTHFR
Come ho detto sopra, le mutazioni del gene MTHFR possono influenzare la capacità del corpo di elaborare gli aminoacidi – in particolare l’omocisteina e il folato – che possono portare a esiti negativi per la salute.
Le condizioni che i ricercatori hanno associato alle mutazioni del gene MTHFR includono:
- omocistinuria (o iperomocistenemia), che è il termine per livelli anormalmente elevati di omocisteina nel sangue o nelle urine
- atassia, una condizione neurologica che influenza la coordinazione
- neuropatia periferica, una condizione neurologica che danneggia i nervi
- microcefalia, una condizione presente alla nascita in cui la testa è più piccola del solito
- scoliosi, un’anomala curvatura della colonna vertebrale
- anemia, cioè una carenza di globuli rossi sani
- malattie cardiovascolari, come coaguli di sangue, ictus e infarti
- disturbi mentali e comportamentali, come depressione e disturbo da deficit di attenzione e iperattività (ADHD )
- Autismo
- Retinoblastoma (tumore dell’occhio più comune in età pediatrica e colpisce quasi esclusivamente bambini di età inferiore ai 4-5 anni)
- carcinoma mammario e recidive dello stesso
- metastasi linfonodali
- malattia coronarica prematura (CAD) e infarto del miocardio (MI)
- Sindrome dell’ovaio policistico (PCOS)
E tante altre problematiche solo da pochi anni la ricerca medica sta scoprendo piano piano.
Possibili segni e sintomi
I sintomi variano sia tra gli individui che a seconda del tipo di mutazione. Le persone di solito non sanno di avere una mutazione MTHFR a meno che non manifestino sintomi gravi o siano sottoposti a test genetici.
Avere una o due mutazioni MTHFR può aumentare i livelli di omocisteina presenti nel sangue o nelle urine, provocando appunto omocistinuria.
L’omocisteina è un aminoacido (cioè uno dei “mattoncini” che costituiscono le proteine) che l’organismo produce scomponendo appunto le proteine alimentari.
Nell’omocistinuria, il corpo non è in grado di scomporre determinate proteine e in particolare, la condizione colpisce un amminoacido chiamato metionina.
Nelle persone sane, l’omocisteina è subito trasformata in altri prodotti grazie all’azione delle vitamine B6 e B12 e dei folati (acido folico).
Se con l’alimentazione si assumono quantità insufficienti di queste vitamine e di acido folico, l’omocisteina si accumula nel sangue e può provocare danni al sistema nervoso, cardiovascolare e osseo.
Infatti, alti livelli di omocisteina sono stati messi in relazione ad un aumento del rischio di sviluppare malattie cardiovascolari anche gravi, quali arteriosclerosi, infarto del miocardio, ictus cerebrale e trombosi.
Gli aminoacidi sono elementi costitutivi umani essenziali, quindi anche la metionina è fondamentale, per esempio per la crescita dei bambini e anche per gli adulti è basilare in quanto regola l’azoto nel corpo.
L’ azoto è importante per il DNA umano, perché tutti gli aminoacidi contengono questa sostanza.
Le persone che hanno alti livelli di omocisteina tendono ad avere bassi livelli di vitamina B-12.
Diversi fattori possono influire sulla quantità di omocisteina nel sangue:
- fattori ambientali, quali il fumo, l’alcol, il caffè e l’inattività fisica
- fattori fisiologici, quali l’età ed il sesso (i livelli di omocisteina sono più bassi nelle donne rispetto agli uomini. Nelle donne si osserva un aumento dopo la menopausa, molto probabilmente dovuto ad una diminuzione degli estrogeni)
- malattie quali insufficienza renale e ipotiroidismo
- assunzione di farmaci (contraccettivi orali, antiepilettici)
- fattori ereditari (omocistinuria)
I sintomi dell’omocistinuria dovuti a mutazioni MTHFR includono:
- coagulazione del sangue anormale
- ritardi nello sviluppo
- convulsioni
- microcefalia
- coaguli di sangue
- scarso coordinamento
- intorpidimento o formicolio alle mani e ai piedi
- Alzheimer e altre demenze
Bambini e omocistinuria
I bambini con omocistinuria hanno dei sintomi che variano da lievi a gravi.
I neonati con tale disturbo sono sani alla nascita. I primi sintomi, compresa la lussazione del cristallino che causa una marcata riduzione della vista, solitamente compaiono dopo i tre anni di età.
La maggior parte dei bambini presenta anomalie scheletriche, quali l’osteoporosi.
I bambini in genere sono magri con colonna vertebrale curva, deformità toraciche, arti oblunghi e aracnodattilia.
La sindrome di Beals, o aracnodattilia contratturale congenita (CCA), è una malattia del tessuto connettivo, caratterizzata da contratture multiple in flessione, aracnodattilia, cifoscoliosi grave, padiglioni auricolari abnormi e ipoplasia muscolare.
In assenza di una diagnosi e un trattamento precoci, sono comuni disturbi comportamentali e mentali (psichiatrici) e deficit intellettivo.
L’omocistinuria aumenta la probabilità che il sangue coaguli spontaneamente, causando ictus, ipertensione arteriosa e molti altri problemi gravi.
Test di screening neonatale
Dal 2008 quasi tutti gli Stati degli Stati Uniti richiedono lo screening di tutti i neonati per l’omocistinuria con un esame del sangue. La diagnosi è confermata mediante un test che misura la funzione enzimatica del fegato ed esami delle cellule cutanee.
In Italia quasi nessuno la controlla, nemmeno da adulti, quindi si consiglia di fare questo semplice esame del sangue entro i primi 5 anni di età o alla comparsa di questi sintomi.
I valori normali di omocisteina devono essere 3-10 μmol/L nel plasma nei ragazzi fino ai 15 anni.
Effetti sulla gravidanza
Le donne che risultano positive per una mutazione MTHFR possono avere un aumentato rischio di preeclampsia (una complicazione della gravidanza potenzialmente pericolosa sia per la mamma sia per il neonato), aborti ricorrenti o dare alla luce un bambino con disabilità congenite.
Una meta-analisi del 2015 ha rivelato prove evidenti che suggeriscono che le donne che hanno genotipi MTHFR C677T hanno un rischio più elevato di preeclampsia.
Secondo i ricercatori, questa mutazione era presente 1,337 volte più spesso tra le donne con preeclampsia.
In uno studio del 2018 i ricercatori hanno scoperto che l’aborto si verificava più frequentemente nelle donne con mutazione MTHFR C677T rispetto a quelle con mutazione MTHFR A1298C.
I ricercatori hanno anche notato forti associazioni tra le varianti MTHFR e i seguenti esiti della gravidanza:
- bambini nati con labbro leporino o palatoschisi (una malformazione congenita del palato, che si presenta come una fenditura più o meno estesa della parte anteriore)
- bambini nati con anomalie cardiovascolari
- bambini nati con anomalie del sistema urinario
- aborti ripetuti
- rottura prematura delle membrane (PPROM)
- ablazione placentare, che è quando la placenta si separa dal rivestimento uterino prima della nascita
- spina bifida, una malformazione del sistema nervoso dovuta alla mancata chiusura del tubo neurale fin dalle prime settimane del concepimento; nei casi più gravi il midollo spinale fuoriesce dalla colonna vertebrale.
Il Centro informazioni sulle malattie genetiche e rare afferma che gli studi suggeriscono che le donne con due varianti del gene C677T potrebbero avere un rischio maggiore di dare alla luce un bambino con un difetto del tubo neurale.
I difetti del tubo neurale si riferiscono a disabilità del cervello, della colonna vertebrale o del midollo spinale presenti alla nascita e di solito si sviluppano durante il primo mese di gravidanza.
Complicazioni
La complicazione più grave dell’omocistinuria sono i coaguli di sangue, che possono essere potenzialmente letali e aumentare il rischio di ictus.
È anche possibile una disabilità intellettuale, ma il rischio può essere ridotto se l’omocistinuria viene diagnosticata precocemente e trattata con successo.
Le lenti slogate degli occhi possono danneggiare la vista. Addirittura, potrebbe essere necessario un intervento chirurgico di sostituzione dell’obiettivo per aiutare alcune persone.
Le persone con omocistinuria possono condurre una vita normale se vengono diagnosticate abbastanza presto e il loro trattamento ha successo. Tuttavia, i coaguli di sangue possono causare problemi di salute e talvolta complicazioni potenzialmente letali.
E’ bene sapere che avere una mutazione MTHFR non influenza tutti allo stesso modo.
Le persone che hanno una o più varianti di MTHFR possono avere livelli di omocisteina più alti del normale nel sangue o nelle urine, ma non è detto che questa situazione possa sfociare nei problemi sopra elencati, mentre in altri si.
Insomma, ognuno è un caso a se.
Quindi approfondisci la questione MTHFR/omocisteina soprattutto questi sintomi dati dalla carenza di folati o vitamina B12, come:
- fatica
- mancanza di respiro
- stipsi
- perdita di appetito o perdita di peso involontaria
- debolezza muscolare
- intorpidimento, formicolio o dolore alle mani o ai piedi
- vertigini o perdita di equilibrio
- piaghe alla bocca
- cambiamenti d’umore
- respiro difficoltoso
- mal di testa
- battito cardiaco irregolare
Omocisteina alta: valori di riferimento
I livelli di omocisteina sono misurati attraverso un campione ematico (cioè con analisi del sangue).
Livelli normali si attestano, per gli adulti tra i 15 e i 65 anni, tra i 5 ed i 15 micromoli per litro (i micromoli sono l’unità di misura delle molecole più piccole).
Oltre si parla di omocisteina alta che ha però diverse sfumature di gravità:
- Sopra i 15-30 micromoli per litro: lieve/ moderata
- 30-100 micromoli per litro: media
- Maggiore di 100 per litro: grave
- Oltre i 65 anni i valori devono essere entro i 3-20 micromoli
- 3-10 micromoli invece nei ragazzi fino ai 15 anni.
- Alcuni studiosi considerano la presenza di omocistinuria già quando il valore supera i 12 micromoli.
L’ omocistinuria severa è rara, mentre la forma moderata è presente nel 5-7 per cento della popolazione generale.
E’ considerata come uno dei più importanti fattori di rischio cardiovascolare, dal momento che livelli superiori al 12% dei valori normali coincidono con un rischio tre volte maggiore di ictus o infarto cardiaco.
L’ omocistinuria è particolarmente frequente nei pazienti con malattie delle coronarie (circa 30 per cento) e in quelli con patologie cerebrovascolari (42 per cento).
Come si può vedere da questa tabella la mortalità per malattie cardio-vascolari nelle varie popolazioni è correlata alla quantità media di omocisteina nel sangue.

Quindi più è alto il valore di questa sostanza e più c’è probabilità di morire per infarti ictus.
Interessante notare che la popolazione dell’Irlanda del Nord ha valori altissimi di omocisteina e quindi, purtroppo, di mortalità cardiovascolare.
Guarda caso, la mutazione MTHFR in questa nazione è tra le più frequenti rispetto al resto del mondo, come vedremo anche dopo nei dati epidemiologici.
Prevalenza
Valori di omocisteina alta nel sangue sono quindi molto pericolosi per la salute e sono presenti in circa il 7-12% della popolazione generale.
In Italia l’omocistinuria colpisce un nuovo nato ogni 1.200.000/1.400.000, mentre negli USA si ritiene abbia un’incidenza di circa 1 su ogni 200.000 a 300.000 bambini ed è più comune tra i bianchi del New England che sono di origine irlandese. In questo gruppo, la condizione colpisce uno su 50.000 neonati.
In tutto il mondo, il tipo più comune di omocistinuria colpisce 1 su 200.000 a 335.000 persone e sembra essere più diffuso in alcuni paesi, tra cui Germania, Norvegia, Irlanda e Qatar.
Cosa fare per scoprire se in possesso di gene/i MTHFR mutati e/o omocisteina alta
- Per l’MTHFR basta fare un semplice test genetico utilizzando un bastoncino per raccogliere un campione di saliva (tipo CSI per intenderci), per esempio>>>QUI
- Per l’omocisteina richiedere l’apposito dosaggio con un normale prelievo di sangue
- Controllare nel caso anche i livelli di folati, la vitamina B6 e la vitamina B12
Ecco quindi le 4 cose che devi assolutamente fare se scopri di avere l’MTHFR mutato e/o l’ omocisteina alta
1) Considerazioni dietetiche
Il gene MTHFR regola il modo in cui il corpo elabora il folato, un aminoacido delle proteine animali e altre vitamine del gruppo B.
Mangiare cibi ricchi di folati può aiutare a ridurre i sintomi dovuti alle mutazioni dell’MTHFR e quindi anche il pericoloso aumento dell’omocisteina.
Ovviamente, è consigliata la GeoPaleoDiet, quindi escludere cereali/latticini/legumi e porre consumare con soprattutto questi cibi ricchi di folati:
- proteine animali e vegetali, come carne di manzo e uova
- verdure, tra cui spinaci, asparagi, cavoletti di Bruxelles e broccoli
- frutti come banana, melone, papaia e avocado
2) Attività fisica
Inserire anche una regolare allenamento con i pesi, a quanto risulta dai dati di uno studio dell’ Università della Virginia (USA).
I ricercatori americani hanno sottoposto due gruppi di persone omogenee dall’ età variante dai 60 ai 72 anni, sia dal peso normale che obesi; un gruppo ha praticato pesi per 6 mesi, mentre l’altro gruppo di controllo è rimasto sedentario.
Alla fine dello studio i livelli omocisteina nel sangue erano più bassi nel gruppo che si era allenato con i sovraccarichi, sia quelli con il peso normale che negli obesi.
Non solo, ma i livelli di perossidazione lipidica, un processo che porta a danneggiare le nostre cellule e accellerare l’invecchiamento, erano più bassi nel gruppo che si era allenato con i pesi.
I ricercatori hanno concluso che:
“A nostra conoscenza, questi dati sono i primi per indicare che il training con i pesi riduce lo sforzo ossidativo indotto dall’ esercizio e i livelli di omocisteina. Questi dati suggeriscono che i pesi possono permettere una certa protezione contro i fattori di rischio cardiovascolari, anche e soprattutto per i soggetti anziani obesi e non”.
3) Prendere tanto sole e/o integratori di Vitamina D
Uno studio pubblicato su Plos One nel 2016, effettuato su 4475 canadesi, ha scoperto che sia le concentrazioni sieriche di vitamina D più elevate al basale, sia i maggiori miglioramenti temporali di incremento nel sangue di questa vitamina con luce solare e/o integratori, erano associati a una riduzione del rischio di omocisteina elevata.
I ricercatori hanno quindi concluso che, conseguentemente, più sole, più vitamina D (anche come integratori) e meno c’è rischio di malattie cardiovascolari.
Vitamina D3 consigliata >>>QUI
4) Integrazione.
In caso di mutazione/i MTHFR e/o omocisteina alta (per alcuni sopra gli 8 micromoli per litro già può essere problematico) assumere un integratore contenente:
- Acido folico ATTIVATO 5-metiltetraidrofolico (quello normale può essere addirittura dannoso)
- Vitamina B2
- Vitamina B6
- Vitamina B12
- Zinco
Prodotto consigliato MTHFR SUPPORT >>>QUI
Guarda anche i miei video QUI:
Tozzipedia: il mio nuovo libro
TOZZIPEDIA è l’enciclopedia definitiva per chi cerca di migliorare la propria salute e il proprio benessere attraverso la dieta e l’esercizio fisico. Questo manuale enciclopedico di Claudio Tozzi, un professionista con oltre 25 anni di esperienza nel campo della dieta Geo Paleo, raccoglie tutte le risorse e le ricerche accumulate nel corso degli anni.
TOZZIPEDIA è un manuale completo che copre un’ampia gamma di argomenti, tra cui la dieta Geo Paleo, l’allenamento, la gestione delle patologie, e le variazioni speciali delle diete. Offre una guida all’integrazione specifica per tutte le condizioni, testimonianze e casi studio a supporto, istruzioni per il raggiungimento di obiettivi specifici, e informazioni rilevanti su trattamenti specifici per problematiche estetiche.
TOZZIPEDIA è stato creato per essere un riferimento per tutti, dai principianti ai professionisti del settore della salute e dell’allenamento. È stato concepito per essere una risorsa di facile utilizzo, con un indice completo per aiutarti a trovare rapidamente le risposte alle tue domande.
Acquistalo >>>QUI
Bibliografia MTHFR:
- Nutrition and Food Sciences Research Vol 2, No 2, AprJun 2015 – Riboflavin Lowers Blood Pressure: A Review of a Novel Gene nutrient Interaction – JJ Strain*Catherine FHughes, Helene McNulty, Mary Ward – http://nfsr.sbmu.ac.ir/article-1-62-en.pdf
- J Thromb Haemost. 2005 Feb;3(2):292-9. Homocysteine, MTHFR and risk of venous thrombosis: a meta-analysis of published epidemiological studies. Den Heijer M1, Lewington S, Clarke R. – https://www.ncbi.nlm.nih.gov/pubmed/15670035
- 2002 Oct 23-30;288(16):2023-31. MTHFR 677C–>T polymorphism and risk of coronary heart disease: a meta-analysis. Klerk M1, Verhoef P, Clarke R, Blom HJ, Kok FJ, Schouten EG; MTHFR Studies Collaboration Group.
- Mol Genet Genomic Med. 2019 Oct 30:e1020. doi: 10.1002/mgg3.1020. Association of MTHFR C677T polymorphism and type 2 diabetes mellitus (T2DM) susceptibility. Meng et altri – https://www.ncbi.nlm.nih.gov/pubmed/31663297
- BMC Med Genet. 2019 Oct 23;20(1):163. doi: 10.1186/s12881-019-0905-9. MTHFR and F5 genetic variations have association with preeclampsia in Pakistani patients: a case control study. Khidri FF1,2, Waryah YM1,3, Ali FK4, Shaikh H1, Ujjan ID5, Waryah AM6,7. https://www.ncbi.nlm.nih.gov/pubmed/31646966
- Asian J Psychiatr. 2019 Sep 23;46:54-61. doi: 10.1016/j.ajp.2019.09.016. Association of MTHFR 677C>T and 1298A>C polymorphisms with susceptibility to autism: A systematic review and meta-analysis. Sadeghiyeh T1, Dastgheib SA2, Mirzaee-Khoramabadi K3, Morovati-Sharifabad M4, Akbarian-Bafghi MJ5, Poursharif Z6, Mirjalili SR7, Neamatzadeh H8. – https://www.ncbi.nlm.nih.gov/pubmed/31614268
- Autism Res. 2013 Oct;6(5):384-92. doi: 10.1002/aur.1300. Epub 2013 May 7.Association between MTHFR gene polymorphisms and the risk of autism spectrum disorders: a meta-analysis.Pu D1, Shen Y, Wu J.
- Fetal Pediatr Pathol. 2019 Oct 1:1-8. doi: 0.1080/15513815.2019.1666330. Association of MTHFR 677C > T and 1298A > C polymorphisms with susceptibility to attention deficit and hyperactivity disorder. Sadeghiyeh T1, Dastgheib SA2, Lookzadeh MH3, Noori-Shadkam M3, Akbarian-Bafghi MJ4, Zare-Shehneh M5, Poursharif Z6, Neamatzadeh H5,7 – https://www.ncbi.nlm.nih.gov/pubmed/31573368
- Indian J Pharmacol. 2019 Jul-Aug;51(4):248-254. doi: 10.4103/ijp.IJP_215_19. Methylenetetrahydrofolate reductase polymorphism in healthy volunteers and its correlation with homocysteine levels in patients with thrombosis. Munshi R1, Panchal F1, Kulkarni V2, Chaurasia A3. – https://www.ncbi.nlm.nih.gov/pubmed/31571711
- Biochem Genet. 2019 Sep 24. doi: 10.1007/s10528-019-09937-x. Association Between MTHFR Gene Common Variants, Serum Homocysteine, and Risk of Early-Onset Coronary Artery Disease: A Case-Control Study. Zhang SY1, Xuan C2, Zhang XC3, Zhu J1, Yue K1, Zhao P1, He GW4,5, Lun LM1, Tian QW6. – https://www.ncbi.nlm.nih.gov/pubmed/31552564
- Breast J. 2019 Sep 23. doi: 10.1111/tbj.13527. Associations between folate metabolism enzyme polymorphisms and breast cancer: A meta-analysis. Mo W1, Ding Y1, Zheng Y1, Zou D1, Ding X1. – https://www.ncbi.nlm.nih.gov/pubmed/31549463
- Mol Biol Res Commun. 2019 Jun;8(2):53-58. doi: 10.22099/mbrc.2019.33006.1393. Investigating the methylation status of DACT2 gene and its association with MTHFR C677T polymorphism in patients with colorectal cancer. Jalilvand A1, Soltanpour MS2.
- Arch Med Res. 2019 May;50(4):175-180. doi: 10.1016/j.arcmed.2019.07.010. Epub 2019 Sep 6. Association Between the 5,10-MTHFR 677C>T and RFC1 80G>A Polymorphisms and Acute Lymphoblastic Leukemia. Gómez-Gómez Y1, Organista-Nava J2, Villanueva-Flores F3, Estrada-Brito JS3, Rivera-Ramírez AB3, Saavedra-Herrera MV3, Jiménez-López MA3, Illades-Aguiar B2, Leyva-Vázquez MA4. – https://www.ncbi.nlm.nih.gov/pubmed/31499477
- Diabetes Metab Syndr Obes. 2019 Jul 23;12:1201-1212. doi: 10.2147/DMSO.S205379. eCollection 2019. Plausible relationship between homocysteine and obesity risk via MTHFR gene: a meta-analysis of 38,317 individuals implementing Mendelian randomization. Fu L1, Li YN1, Luo D1,2, Deng S1, Hu YQ1,3. – https://www.ncbi.nlm.nih.gov/pubmed/31413611
- Rom J Ophthalmol. 2019 Apr-Jun;63(2):107-118. Association of MTHFR C677T and A1298C Polymorphisms with Glaucoma Risk: a Systematic Review Meta-Analysis based 42 Case-Control Studies. Gohari M1, Mirjalili SA2, Akbarian-Bafghi MJ3, Jarahzadeh MH4, Zare-Shehneh M2, Neamatzadeh H2. – https://www.ncbi.nlm.nih.gov/pubmed/31334388
- J Gene Med. 2019 Sep;21(9):e3114. doi: 10.1002/jgm.3114. Epub 2019 Aug 6. Methylenetetrahydrofolate reductase polymorphisms and colorectal cancer prognosis: A meta-analysis. Chen XL1, Wang YM2, Zhao F1, Chen Z3, Yang X4, Sun C5, Gao Y6, Yang TG7, Tian G7, Chen YM1, Zhu SL8, Lin XB9, Liu FB8 – https://www.ncbi.nlm.nih.gov/pubmed/31330573
- 2019 Nov 30;719:144079. doi: 10.1016/j.gene.2019.144079. Epub 2019 Aug 24. Association of methylenetetrahydrofolate reductase C677T and A1298C polymorphisms with genetic susceptibility to polycystic ovary syndrome: A PRISMA-compliant meta-analysis. Zhu X1, Hong X1, Chen L1, Xuan Y1, Huang K1, Wang B2. – https://www.ncbi.nlm.nih.gov/pubmed/31454542
- 2017 Jun 14;8(35):59509-59517. doi: 10.18632/oncotarget.18472. eCollection 2017 Aug 29. Methylenetetrahydrofolate reductase C677T polymorphism and the risks of polycystic ovary syndrome: an updated meta-analysis of 14 studies. Wang L1, Xu W1, Wang C1, Tang M2, Zhou Y2. – https://www.ncbi.nlm.nih.gov/pubmed/28938654
- Klin Onkol. 2019 Fall;32(5):375-379. doi: 10.14735/amko2019375. Association of MTHFR 677C>T, 1298A>C and MTR 2756A>G Polymorphisms with Risk of Retinoblastoma. Gohari M, Dastgheib S. A., Jafari-Nedooshan J, Akbarian-Bafghi M. J., Morovati-Sharifabad M, Mirjalili S. R., Neamatzadeh H. – https://www.ncbi.nlm.nih.gov/pubmed/31610671
- 2019 Jun 27;11(6):e5014. doi: 10.7759/cureus.5014. Methylenetetrahydrofolate Reductase Polymorphism and Premature Coronary Artery Disease. Zaghloul A1, Iorgoveanu C1, Desai A1, Balakumaran K2, Chen K2. – https://www.ncbi.nlm.nih.gov/pubmed/31497444
- Nutr Cancer. 2019;71(7):1055-1060. doi: 10.1080/01635581.2019.1577985. Epub 2019 Jul 8. Correlation Between MTHFR Polymorphisms and Hepatocellular Carcinoma: A Meta-analysis. Su H1. – https://www.ncbi.nlm.nih.gov/pubmed/31282757
- Ann Nutr Metab. 2019;74(3):251-256. doi: 10.1159/000496428. Epub 2019 Mar 27. – Correlation between Methylenetetrahydrofolate Reductase Polymorphisms and Hepatocellular Carcinoma: A Meta-Analysis. Su H1, Zhang G2. – https://www.ncbi.nlm.nih.gov/pubmed/30917367
- Int J Med Sci. 2019 Jul 22;16(8):1089-1095. doi: 10.7150/ijms.32162. eCollection 2019. Polimorfismi di metilenetetraidrofolato reduttasi ( MTHFR ) C677T e A1298C nel carcinoma mammario: uno studio caso-controllo preliminare sardo. Castiglia P 1 , Sanna V 2 , Azara A 1 , De Miglio MR 1 , Murgia L 1 , Pira G 1 , Sanges F 1 , Fancellu A 1 , Carrello C 3 , Bisail M 4 , Muroni MR 1 . – https://www.ncbi.nlm.nih.gov/pubmed/31523170
- J Biomed Res. 2012 Mar;26(2):77-83. doi: 10.1016/S1674-8301(12)60015-3. MTHFR C677T polymorphisms are associated with aberrant methylation of the IGF-2 gene in transitional cell carcinoma of the bladder. Cheng H1, Deng Z, Wang Z, Zhang W, Su J. – https://www.ncbi.nlm.nih.gov/pubmed/23554734
- Proc Nutr Soc. 2019 Aug;78(3):449-462. doi: 10.1017/S0029665119000661. Epub 2019 Jun 3. Addressing optimal folate and related B-vitamin status through the lifecycle: health impacts and challenges. McNulty H1, Ward M1, Hoey L1, Hughes CF1, Pentieva K1. – https://www.ncbi.nlm.nih.gov/pubmed/31155015
- Clin Nutr ESPEN. 2019 Apr;30:199-203. doi: 10.1016/j.clnesp.2019.01.009. Epub 2019 Feb 12. Association of vitamin B12 mediated hyperhomocysteinemia with depression and anxiety disorder: A cross-sectional study among Bhil indigenous population of India. Saraswathy KN1, Ansari SN2, Kaur G3, Joshi PC4, Chandel S5. – https://www.ncbi.nlm.nih.gov/pubmed/30904222
- Fertil Steril. 2003 Nov;80(5):1190-4. C677T methylenetetrahydrofolate reductase polymorphism interferes with the effects of folic acid and zinc sulfate on sperm concentration. Ebisch IM1, van Heerde WL, Thomas CM, van der Put N, Wong WY, Steegers-Theunissen RP. https://www.ncbi.nlm.nih.gov/pubmed/14607573
- J Gynecol Obstet Hum Reprod. 2019 Aug 22. pii: S2468-7847(19)30058-3. doi: 10.1016/j.jogoh.2019.08.005. 5-Methyltetrahydrofolate reduces blood homocysteine level significantly in C677T methyltetrahydrofolate reductase single-nucleotide polymorphism carriers consulting for infertility. Clément A1, Menezo Y2, Cohen M3, Cornet D4, Clément P5. – https://www.ncbi.nlm.nih.gov/pubmed/31446167
- Reprod Toxicol. 2017 Sep;72:159-163. doi: 10.1016/j.reprotox.2017.07.001. Epub 2017 Jul 6. The importance of folate, vitamins B6 and B12 for the lowering of homocysteine concentrations for patients with recurrent pregnancy loss and MTHFR mutations. Serapinas D1, Boreikaite E2, Bartkeviciute A2, Bandzeviciene R3, Silkunas M2, Bartkeviciene D2. – https://www.ncbi.nlm.nih.gov/pubmed/28689805
- Yan L et al. (2012). “Association of the maternal MTHFR C677T polymorphism with susceptibility to neural tube defects in offsprings: evidence from 25 case-control studies.” PLoS One. 7(10):e41689. https://www.ncbi.nlm.nih.gov/pubmed/23056169
- Yang Y et al. (2015). “Association between MTHFR C677T polymorphism and neural tube defect risks: A comprehensive evaluation in three groups of NTD patients, mothers, and fathers.” Birth Defects Res A Clin Mol Teratol. 103(6):488-500. https://www.ncbi.nlm.nih.gov/pubmed/25808073
- Crider KS et al. (2011). “Folic acid food fortification-its history, effect, concerns, and future directions.” Nutrients. 3(3):370-84. https://www.ncbi.nlm.nih.gov/pubmed/22254102 [14]Hickey SE et al. (2013). “ACMG Practice Guideline: lack of evidence for MTHFR polymorphism testing.” Genet Med. 15(2):153-6. https://www.ncbi.nlm.nih.gov/pubmed/23288205 [15]American College of Obstetricians and Gynecologists Women’s Health Care Physicians. (2013). “ACOG Practice Bulletin No. 138: Inherited thrombophilias in pregnancy.” Obstet Gynecol. 122(3):706-17. https://www.ncbi.nlm.nih.gov/pubmed/23963422 [16]Genetics Home Reference. “Homocystinuria.” https://ghr.nlm.nih.gov/condition/homocystinuria
- PLoS One . 2016; 11 (8): e0161368. Pubblicato online il 22 agosto 2016 : doi: 1371 / journal.pone.0161368 – PMCID: PMC4993504 – PMID: 27548258 L’effetto della siero 25-idrossivitamina D sulle concentrazioni elevate di omocisteina nei partecipanti a un programma di salute preventiva – Truong-Minh Pham , John Paul Ekwaru , Silmara S. Mastroeni , Marco F. Mastroeni , Sarah A. Loehr ,e Paul J. Veugelers *




